基盤研究部門
老化・代謝疾患コアセンター
超高齢化社会を迎え、肥満を背景としたメタボリックシンドローム・糖尿病・高血圧・動脈硬化・糖尿病性合併症・脂肪性肝障害などの代謝異常や加齢に伴う疾患に関する研究は、健康な寿命の延伸に重要な分野となっております。本コアセンターでは、これらの疾患の病因解明と画期的治療法の開発を目標に、東北大学のさまざまな分野(医学系研究科、病院、メディカルメガバンク機構、薬学研究科、医工学研究科、加齢医学研究所、学際科学フロンティア研究所、未来型医療創成センターなど)の最先端の研究者が結集し、学際的・融合的に代謝疾患の研究を展開します。積極的な共同研究による異分野融合そしてビッグデータ取得、インフォマティクス解析による新たな視点から代謝疾患研究を世界に発信する重要な拠点へと発展させたいと考えています。
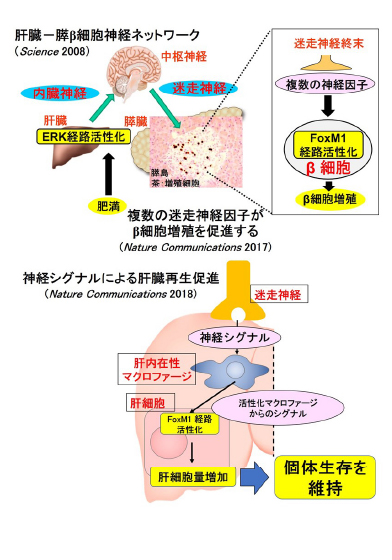
糖尿病や脂質異常症などの代謝疾患は加齢と共に病態が悪化し、高齢者における有病率の増加につながっていると考えられます。このことからこれら疾患の病態解明、治療法開発を行うためには代謝疾患と老化について統合的な取り組みを進める必要があります。私はこれまで自律神経シグナルを介した全身の代謝調節機構についての研究を行ってきました。本コアセンターでは、東北大学の様々な分野と協調しつつ、神経シグナルによる代謝調節メカニズムを明らかにし、代謝疾患の病態解明を進めるとともに、加齢に伴うこれら調節メカニズムの変容を解析することで、老化の本質に迫りたいと考えています。また、本来体に備わっているこれらのシステムを利用したこれまでにない代謝疾患の治療法開発を目指します。
コアセンター概要
栄養や環境からの刺激は神経やホルモンを介して標的となる臓器へと伝えられ、さらに細胞内シグナル伝達を介して、核内情報(エピゲノムなど)に変換され、遺伝子発現を介して細胞の代謝などの機能が調節されております。また、それぞれの臓器はばらばらに代謝を行うのではなく、神経やホルモンを介した仕組みによって連携され、恒常性を保つように制御されています。この制御破綻が肥満・糖尿病などの代謝疾患です。我々は次世代シーケンサーや質量分析などにより核内データを取得し、ビッグデータのインフォマティクス解析などにより核内情報を分析し、臓器間の代謝連携システム、核内情報システムに基づく代謝疾患の画期的治療法の開発を目指します。
コアセンター研究紹介
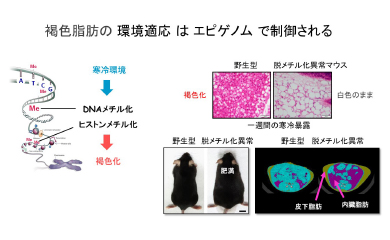
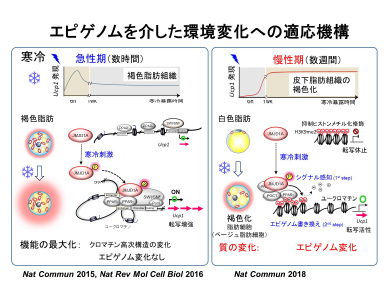
「環境刺激はどのように感知され、エピゲノム変化を介して体質を形成し、肥満・代謝性疾患(生活習慣病)を発症に至るのか」の研究をエピゲノム解析と核内情報のインフォマティクス解析から進めています。これまで、遺伝子発現に促進と抑制と相反する機能を示す2種類の異なるヒストン修飾をもつクロマチン構造が刺激によって転写促進の構造変化をとり、脂肪細胞分化を最終的に決定する仕組み (Mol Cell 2015) や、また環境変化を感知するエピゲノム酵素による急性と慢性の環境変化に対して異なる細胞で異なる機構によるステップワイズな適応機構の解明などをしてきております(Nat Commun 2015, 2018, Nat Rev Mol Cell Biol, 2016)。
コアセンター関連画像
コアセンターメンバー
- 酒井 寿郎教授分子代謝生理学分野
- 今井 淳太准教授糖尿病代謝内科学分野
- 伊藤 亮助教分子代謝生理学分野
- 高橋 宙大助教分子代謝生理学分野
- 魏 范研教授加齢医学研究所 モドミクス医学分野
- 小川 亜希子助教加齢医学研究所 モドミクス医学分野
- 松田 盛助教加齢医学研究所 モドミクス医学分野
- 松井 広教授生命科学研究科 超回路脳機能分野
- 堀内 久徳教授加齢医学研究所 基礎加齢研究分野
- 白川 龍太郎助教加齢医学研究所 基礎加齢研究分野